
Turinys
- etapai
- 1 metodas Lygties subalansavimas bandymų ir klaidų metodu
- 2 metodas Išlyginkite lygtį algebriniu metodu
Chemijoje lygtis nustato, kas nutiko cheminės reakcijos metu. Į kairę nuo lygties dedame reagentus, kurie buvo naudojami eksperimentui, o dešinėje - produktus, gautus eksperimento metu. Pagal masės išsaugojimo principą (Lavoisier) vykstant cheminei reakcijai, nė vienas atomas neišnyksta, nė vienas nesukuriamas, jie sujungiami skirtingai. Apibendrinant reikia pasakyti, kad kiekvieno elemento dešimtainėje dalyje turi būti tokie patys skaičiaus duomenys kaip lygties kairėje. Štai kodėl pusiausvyros lygtis visada turi būti subalansuota.
etapai
1 metodas Lygties subalansavimas bandymų ir klaidų metodu
-
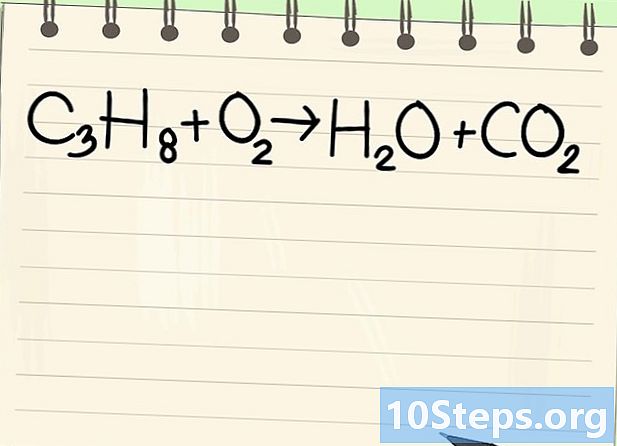
Atkreipkite dėmesį į pusiausvyros lygtį. Mes traktuosime šią lygtį:- C3O8 + O2 -> H2O + CO2
- Tai yra propano degimo lygtis (C3O8) deguonyje: gaunamas vanduo ir anglies dioksidas.
-
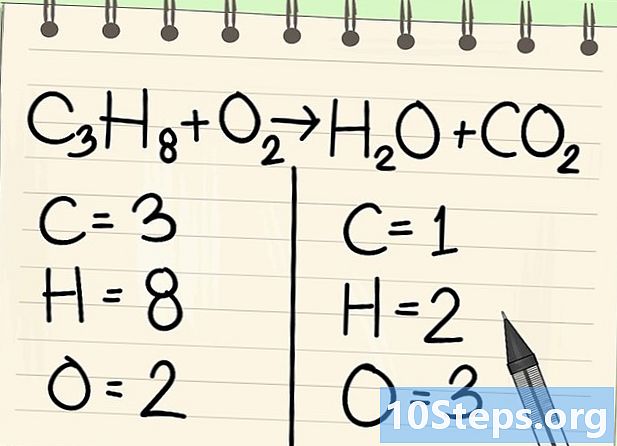
Suskaičiuokite atomus. Įveskite kiekvieno elemento duomenų skaičių vienoje lygties pusėje, po to - kitoje. Tam reikia atsižvelgti į indeksus, jei jų nėra, indeksas yra 1.- Kairėje yra 3 anglies atomai, 8 vandenilis ir 2 deguonis.
- Dešinėje yra 1 anglies atomas, 2 vandenilis ir 3 deguonis.
-
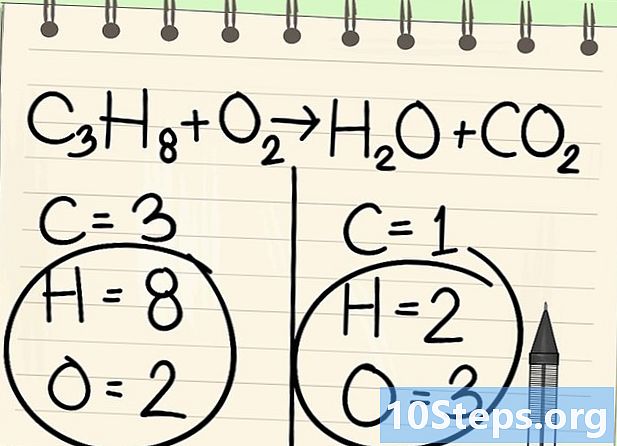
Nedelsdami palikite vandenilį ir deguonį. -

Pradėkite balansuoti su tinkamu elementu. Mes visada pradedame nuo to, kuris yra molekulėje prieš ir po reakcijos. Jei jų yra keli, paimkite tą, kuris vienoje iš molekulių yra lygus. Čia mes pradedame nuo anglies atomų. -

Subalansuokite anglies atomus. Dešinėje pridėkite koeficientą prie anglies dioksido molekulės (CO2), kuriame vien anglies latomas yra. Mes įdėsime 3, kad gautume 3 likusius atomus.- C3O8 + O2 -> H2O + 3CO2
- Taigi koeficiento (3CO) dėka dešinėje yra 3 anglies atomai2) ir 3 anglies atomai kairėje dėka indekso (C3O8).
- Į lygtį galite sudėti visus norimus koeficientus, bet negalima liesti įkalčių.
-
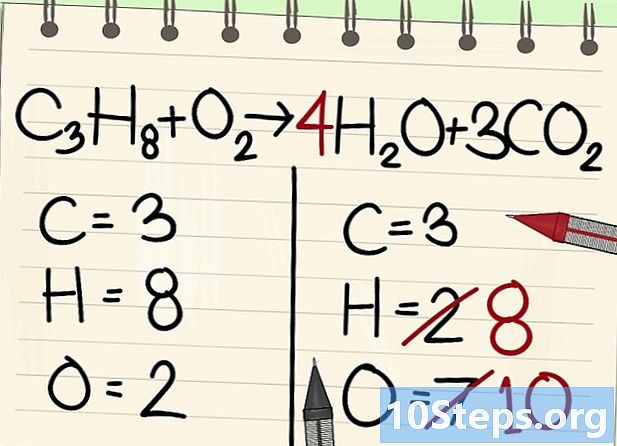
Subalansuokite vandenilio atomus. Kadangi iš lygties turite 8 kairę, jums reikia tiek dešinės.- C3O8 + O2 --> 4O2O + 3CO2
- Dešinėje jūs užduosite koeficientą 4, nes vandenilis yra dvivalentis vandens molekulėje: rodyklė 2 rodo, kad du vandenilio atomai yra susiję.
- Norėdami gauti vandenilio atomų skaičių dešinėje, koeficientą 4 padauginkite iš indekso 2 arba 8 atomų.
- Deguonies atomų dešinėje dabar yra 6 vienoje pusėje, gaunami iš trijų 3CO molekulių2 (3 x 2 = 6 atomai) ir 4 iš 4 H molekulių2O (4 x 1 = 4 atomai), ty iš viso 10 deguonies atomų.
-
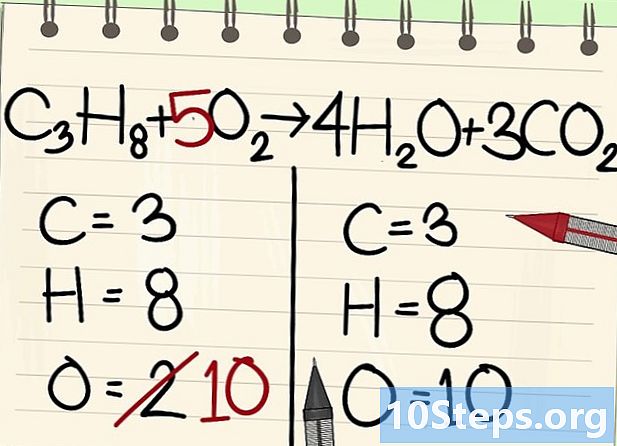
Subalansuokite deguonies atomus.- Dėl anglies ir vandenilio pusiausvyros deguonies atomų skaičius abiejose lygties pusėse nėra vienodas. Anksčiau matėme, kad dešinėje yra 10 deguonies atomų (4 iš vandens molekulių ir 6 iš anglies dioksido molekulių). Kairėje yra tik 2 (iš O2).
- Norėdami subalansuoti deguonį, kairiąją deguonies molekulę pridėkite 5 koeficientą: kairėje turite 10 deguonies atomų, o dešinėje - kitą.
- C3O8 + 5O2 -> 4H2O + 3CO2
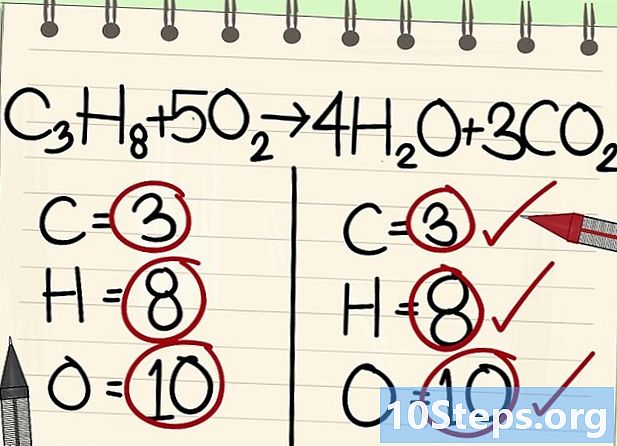
- Visi atomai (anglis, vandenilis ir deguonis) yra subalansuoti: jūsų lygtis yra subalansuota.
2 metodas Išlyginkite lygtį algebriniu metodu
-

Parašykite lygtį, kad subalansuotumėte. Kiekvienai molekulei priskirkite pažodinį koeficientą. Mes jiems paskambinsime turi, b, c ir d. -
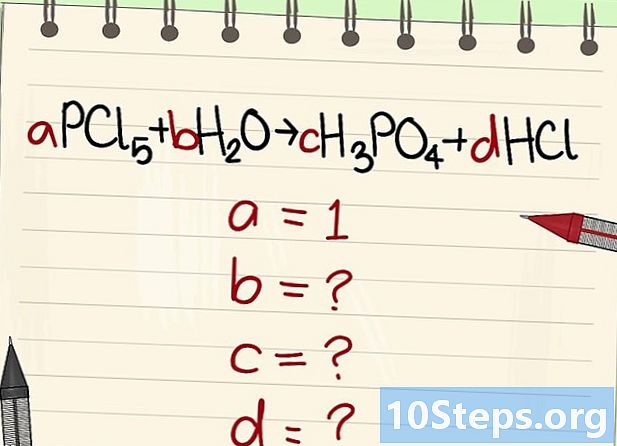
Raskite kitų pažodinių koeficientų vertę. Mes to paklausime turi = 1. -

Raskite šių koeficientų ryšius. Žiūrėdami į kairę (reagentai) ir į dešinę (produktai), nustatykite šių skirtingų koeficientų ryšius.- Paimkite šią lygtį: aPCl5 + bH2O = cH3PO4 + dHCl. Teigta, kad a = 1, tai reiškia, kad c = a, d = 5a ir 2b = 3c + d. Atlikti skaičiavimai, c = 1, d = 5 ir b = 4.

- Paimkite šią lygtį: aPCl5 + bH2O = cH3PO4 + dHCl. Teigta, kad a = 1, tai reiškia, kad c = a, d = 5a ir 2b = 3c + d. Atlikti skaičiavimai, c = 1, d = 5 ir b = 4.


